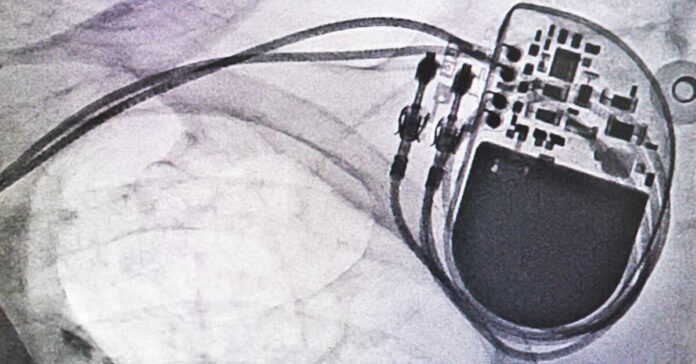
Pajisjet e dëmtuara të zemrës kushtojnë shtrenjtë për Medicare, konsumatorët
Lajme shëndetësore
Pajisjet e dëmtuara të zemrës kushtojnë shtrenjtë për Medicare, konsumatorët
Zyrtarët e FDA njoftojnë procedura të reja testimi për pajisjet e implantueshme të zemrës pasi u zbulua se Medicare ka shpenzuar 1.5 miliardë dollarë për të zëvendësuar pajisjet me defekt.
Gjatë dekadës së fundit Medicare ka shpenzuar më shumë se 1.5 miliardë dollarë për të zëvendësuar pajisjet e zemrës me defekt për 73,000 pacientë.
Kjo është sipas nje raport nga Zyra e Inspektorit të Përgjithshëm (OIG) të Shëndetësisë dhe Shërbimeve Njerëzore (HHS).
OIG është një organizatë e mandatuar për të mbrojtur integritetin e programeve HHS, duke përfshirë Medicare dhe Administratën Amerikane të Ushqimit dhe Barnave (FDA).
Megjithatë, disa nga kostot për heqjen e pajisjeve të dëmtuara të zemrës kanë rënë për konsumatorët.
Sipas raportit, shpenzimet nga xhepi në lidhje me tërheqjet e pajisjeve arritën në 140 milionë dollarë gjatë së njëjtës periudhë.
Raporti i inspektorit të përgjithshëm fokusohet në kostot që lidhen me tërheqjen e shtatë pajisjeve të zemrës, duke përfshirë stimuluesit e ritmit dhe defibrilatorët e implantueshëm për trajtimin e rrahjeve të çrregullta të zemrës, që kishin defekte serioze ose kishin dështuar para kohe.
Raporti përfshin rekomandime për t’i bërë spitalet dhe ofruesit e kujdesit shëndetësor të dorëzojnë informacion të detajuar që identifikon pajisjet e dështuara gjatë procesit të faturimit për të identifikuar më shpejt pajisjet me performancë të dobët.
Ai gjithashtu rekomandon kodim më të mirë në procedurat e tërhequra në lidhje me pajisjen.
“Ka një kod në faturimin e Medicare që tregon prova të një pajisjeje të tërhequr,” tha për Healthline Dr. Rita Redberg, një kardiologe e Universitetit të Kalifornisë në San Francisko (UCSF) që këshillon Medicare. “Por spitalet nuk po e përdorin atë. Përdorimi i atij kodi mund ta zhvendosë faturimin te prodhuesit e pajisjes. Ata duhet të paguajnë në vend të Medicare dhe pacientit.”
Edhe kur përdoret kodi i faturimit për tërheqjen e pajisjes, Medicare zakonisht nuk rimbursohet për kostot e zëvendësimit.
“Ka disa përqind të rasteve kur përdoret ai kod, por prodhuesi ia jep paratë spitalit dhe jo Medicare,” shpjegoi Redberg.
Tërheqja e pajisjeve të zemrës është urdhëruar për probleme të tilla si dështimi i baterive, instalimet elektrike të fragmentuara dhe komponentët që shpërbëhen.
Në një rast, St. Jude Medical (tani në pronësi të Abbott Pharmaceuticals) njoftuar mjekët të një baterie me defekt në 400,000 defibrilatorë të terapisë së risinkronizimit kardiak (CRT-Ds) në tetor 2016.
Kjo ishte pesë vjet pasi Shën Jude mësoi për problemet e baterisë me pajisjet, sipas
Kohët e fundit, Abbott lëshoi
“Shumë nga këto pajisje përfundojnë duke u tërhequr,” tha Redberg. “Përveç kostove, është e rrezikshme dhe e rrezikshme të kesh një procedurë për zëvendësimin e një pajisjeje me defekt.”
Tërheqja e kaq shumë pajisjeve të zemrës tregon vështirësinë e natyrshme në testimin adekuat.
Megjithëse FDA kërkon testime të fuqishme të farmaceutikëve, pajisjet e zemrës i nënshtrohen një shqyrtimi të ndryshëm.
Kur u kontaktua nga Healthline, zyra e shtypit e FDA-së iu përgjigj pyetjeve të ngritura nga raporti i OIG përmes emailit.
Sipas FDA, pajisjet e zemrës kanë nevojë për miratimin e agjencisë bazuar në llojin e pajisjes.
Për shembull, do të ishte një gjenerator implantues impulsesh për një stimulues kardiak subjekt për miratimin para shitjes si një pajisje e klasit III (me rrezik të lartë).
Vargu i tërheqjeve në dekadën e fundit mund të tregojë se duhet të zbatohen masa testimi shtesë për të siguruar besueshmërinë e pajisjes.
FDA, megjithatë, sugjeron që rritja e tërheqjeve midis 2003 dhe 2012 e përmendur në raportin e OIG është rezultat i rritjes së ndërgjegjësimit për njoftimet e tërheqjes – jo një rritje në pajisjet me defekt.
“Për më tepër, këto ndërveprime”, ose kujton, “shkaktuan përpjekje brenda industrisë për të përmirësuar sigurinë e pajisjeve, të cilat pritet të përmirësojnë performancën e pajisjes me kalimin e kohës”, tha agjencia për Healthline.
FDA gjithashtu i tha Healthline se po punon për të zhvilluar
Agjencia tha se tashmë ka investuar 20 milionë dollarë në përpjekje.
Dhe më 24 tetor, komisioneri i FDA Scott Gottlieb
Duke përmendur zhvillimin e mjeteve më moderne të matjes që do të ndihmonin në vendimet rregullatore, FDA pret të minimizojë përdorimin e studimeve të kafshëve, të zvogëlojë kohëzgjatjen e testimit dhe të kërkojë më pak pacientë në studimet klinike.
Këta hapa nxisin inovacionin, por gjithashtu mund të rrisin rrezikun e implantimit të pajisjeve të zemrës me defekt te pacientët për shkak të testimit të kufizuar.