Lajme shëndetësore
FDA miraton terapinë e re të kancerit CAR T për formën e mielomës së shumëfishtë


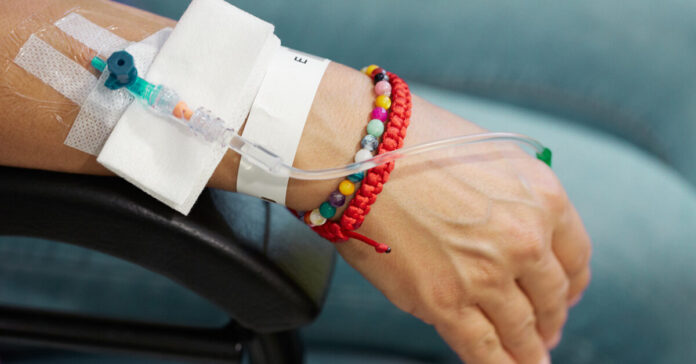
Miquel Llonch/Stocksy United
- Rregullatorët federalë kanë miratuar një ilaç të ri të kancerit CAR T si një trajtim për forma të caktuara të mielomës së shumëfishtë.
- Ekspertët e kancerit thonë se miratimi i cilta-cel do të ofrojë më shumë opsione për njerëzit që nuk janë përgjigjur me sukses ndaj trajtimeve të tjera për mielomë të shumëfishtë.
- Trajtimet CAR T përdorin qelizat T të modifikuara gjenetikisht të një personi për të luftuar kancerin.
Administrata e Ushqimit dhe Barnave (FDA) ka dhënë dritën jeshile në cilta-cel, një trajtim kanceri për njerëzit me mielomë të shumëfishtë të paratrajtuar.
Ilaçi do të shitet me emrin e markës Carvytki. Është prodhuar nga Janssen Pharmaceuticalsnjë kompani në pronësi të Johnson & Johnson.
Është terapi e dytë e tillë miratuar për mielomë të shumëfishtë me miratimin e Bristol Myers Squibb’s Abekma vitin e kaluar.
“Aprovimi i FDA i Carvykti [cilta-cel] shënon terapinë e parë qelizore të miratuar për Janssen, një testament për angazhimin tonë të vazhdueshëm në onkologji për të ofruar opsione të reja terapeutike dhe për të nxitur drejt vizionit tonë për eliminimin e kancerit. Mark WildgustPhD, nënkryetar i çështjeve globale mjekësore për onkologjinë në Janssen, tha për Healthline,
Cilta-cel është pjesë e botës në zgjerim të imunoterapisë së qelizave T të receptorit kimerik të antigjenit, e njohur gjithashtu si terapia CAR T.
MAKINA T përdor qelizat T të modifikuara gjenetikisht të një personi për të gjetur dhe vrarë kancerin.
Ekspertët në fushën e trajtimit të kancerit përshëndetën këtë miratim të fundit të FDA.
Dr. Joseph Mikhaelshefi mjekësor i Fondacionit Ndërkombëtar të Myeloma dhe një profesor në Qendrën e Kancerit City of Hope në Kaliforni, tha për Healthline se miratimi i cilta-cel është një hap i madh përpara.
“Ne tashmë kemi një produkt CAR T-cell të miratuar, por me cilta-cel shkalla e përgjigjes është trefishuar dhe është treguar më e qëndrueshme se terapitë e tjera,” tha Mikhael.
Ai parashikoi se CAR T si cilta-cel si dhe të tjera që janë në linjë do të kenë një rol gjithnjë e më të madh në mielomë.
“Ndoshta edhe në fazat e hershme të sëmundjes,” tha ai. “Ka një entuziazëm të jashtëzakonshëm. Edhe një hematolog geek si unë, nofulla ime bie në dysheme kur shoh se çfarë mund të bëjë ky trajtim.”
Dr. Caitlin Costellonjë onkolog në Qendrën e Kancerit Moores në Universitetin e Kalifornisë San Diego Health, i tha Healthline se CAR T ofron të paktën remisione dhe kura të qëndrueshme në disa raste dhe lejon intervale të gjata pa trajtim.
“Kjo është veçanërisht emocionuese për një kancer si mieloma e shumëfishtë që në thelb ka kërkuar trajtim të vazhdueshëm dhe të pacaktuar për të ruajtur remisionet, të cilat megjithëse janë të suksesshme, mund të kenë implikime klinike dhe financiare,” tha ajo.
Miratimi i FDA ishte rezultat i të dhënave të provave klinike paraqitur në takimin vjetor të Shoqatës Amerikane të Hematologjisë në Atlanta, Gjeorgji, në dhjetor.
Ai provë tregoi se 83 përqind e pjesëmarrësve arritën një përgjigje të plotë në një ndjekje mesatare prej 22 muajsh.
Klinikët gjithashtu raportuan se 92 për qind e pacientëve të vlerësuar arritën negativitet minimal të mbetur të sëmundjes me mbijetesë pa progres dhe mbijetesë të përgjithshme të qëndrueshme në ata pjesëmarrës për më shumë se 6 muaj.
Njerëzit me mielomë të shumëfishtë, për të cilët të paktën tre regjime trajtimi kanë ndaluar së funksionuari, përballen me një mbijetesë mesatare prej më pak se një vit me trajtimet aktualisht të disponueshme.
Dr. Sen Zhuangnënkryetari i kërkimit dhe zhvillimit klinik në Janssen Research & Development, kompania që prodhon cilta-cel, tha se provat klinike ishin një lajm shpresëdhënës për njerëzit me këtë lloj kanceri.
“Këto të dhëna i shtohen numrit në rritje të provave që mbështesin përfitimin e mundshëm klinik të cilta-cel në trajtimin e pacientëve me mielomë të shumëfishtë të relapsuar dhe/ose refraktare, një popullatë që ka nevojë për opsione të reja,” tha Zhuang në një. deklaratë për shtyp ne dhjetor.
Dr. Thomas G. Martinnjë hetues kryesor i studimit dhe drejtor i kërkimit klinik në Qendrën Gjithëpërfshirëse të Kancerit të Familjes Helen Diller të Universitetit të Kalifornisë në San Francisko, dhe hetuesi kryesor i studimit, ishte gjithashtu optimist.
“[The study data] bazuar në rezultatet e mëparshme që tregojnë se një infuzion i vetëm i cilta-cel rezultoi në përgjigje të qëndrueshme dhe mbijetesë afatgjatë në të gjithë popullatën e studimit, duke konfirmuar më tej potencialin e cilta-cel për t’u ofruar pacientëve dhe mjekëve një mundësi të re të vlefshme trajtimi,” Martin tha në atë kohë.
Terapitë CAR T po krijojnë një paradigmë të re për trajtimet e kancerit të gjakut.
Në tetor, FDA
Miratimi, i dyti për Tecartus, u bazua në rezultatet e një prove klinike me më shumë se 50 të rritur që u trajtuan me ilaçin.
Brenda 3 muajve nga marrja e trajtimit, më shumë se gjysma e pjesëmarrësve nuk kishin asnjë shenjë kanceri.
“Ne nuk kemi parë përgjigje dhe kohëzgjatje të përgjigjeve si kjo,” Dr Bijal Shahnjë anëtar i asociuar në departamentin e hematologjisë në Qendrën e Kancerit Moffitt në Florida, i cili ishte hetuesi kryesor i provës klinike,
Trajtimet CAR T kanë pasur disa efekte anësore serioze në të kaluarën, por ekspertët mjekësorë thonë se po i marrin ato nën kontroll.
“Sa i përket sindromës së çlirimit të citokinës dhe neurotoksicitetit, këto janë efekte anësore të njohura të terapisë që mjekët janë bërë shumë të qetë në menaxhimin e tyre. Vlerësimi i vazhdueshëm i qasjeve parandaluese për CRS/neurotoks gjithashtu do të zbusë këto efekte anësore dhe do të lejojë përshtatshmëri më të gjerë për këto trajtime, “tha Costello.
Këtu është një përmbledhje e shkurtër e terapive CAR T që janë miratuar më parë dhe tani janë të disponueshme.
- Abekma nga Bristol Myers Squibb është për të rriturit me mielomë të shumëfishtë recidive ose refraktare pas katër ose më shumë linjave të mëparshme të terapisë.
- Breyanzi nga Bristol Myers Squibb është për të rriturit me limfomë të madhe të qelizave B të relapsuara ose refraktare pas dy ose më shumë linjave të terapisë sistemike.
- Kymriah nga Novartis është për të rriturit me limfomë të madhe të qelizave B të recidivuara ose refraktare dhe të rinjtë deri në 25 vjeç me leuçemi akute limfoblastike të recidivuar ose refraktare.
- Tecartus nga Kite, një kompani Gilead, është për njerëzit me limfomë të qelizës së mantelit të relapsuar ose refraktare. Tecartus është gjithashtu për të rriturit me leuçemi akute limfoblastike pararendëse të qelizave B të relapsuara ose refraktare.
- Yescarta nga Kite, një kompani Gilead, është për njerëzit me limfomë të madhe me qeliza B ose limfomë folikulare.
Standardet e Kontrollit të Fakteve të Healthline News
Ekipi i Healthline News është i përkushtuar të ofrojë përmbajtje që i përmbahet nivelit më të lartë standardet editoriale për saktësinë, burimin dhe analizën objektive. Çdo artikull lajmesh kontrollohet tërësisht nga anëtarët e grupit tonë Rrjeti i Integritetit. Për më tepër, ne kemi një politikë të tolerancës zero në lidhje me çdo nivel plagjiaturë ose qëllimi keqdashës nga shkrimtarët dhe kontribuesit tanë.
Të gjithë artikujt e Healthline News u përmbahen standardeve të mëposhtme:
- Të gjitha studimet dhe punimet kërkimore të referuara duhet të jenë nga revista ose shoqata akademike me reputacion dhe përkatëse të vlerësuara nga kolegët.
- Të gjitha studimet, citimet dhe statistikat e përdorura në një artikull lajmesh duhet të lidhen ose t’i referohen burimit origjinal. Artikulli duhet gjithashtu të tregojë qartë se pse çdo statistikë e paraqitur është e rëndësishme.
- E gjithë përmbajtja që lidhet me trajtime të reja, medikamente, procedura e kështu me radhë duhet të përshkruajë qartë disponueshmërinë, çmimin, efektet anësore, objektivin e trajtimit (p.sh., HER2+), ndërveprimet e njohura dhe përdorimin jashtë etiketës, nëse është e përshtatshme.
- Të gjithë artikujt e lajmeve duhet të përfshijnë komente origjinale nga të paktën dy burime të kualifikuara me kredencialet e duhura dhe lidhje me shoqatat përkatëse ose vepra të botuara.
- Çdo konflikt i mundshëm interesi në lidhje me një studim ose burim duhet t’i tregohet qartë lexuesit.
- Të gjithë artikujt e lajmeve duhet të përfshijnë informacionin dhe kontekstin e duhur të sfondit për gjendjen ose temën specifike.